면역억제 질병의 관리
면역세포들 생성되고 성숙하며 활동하는 장소가 닭의 면역장기
중간독 플러스 백신 감보로병 감염위협 더 높은 상황에서 사용
면역억제 질병은 무엇보다 백신 접종 골자로 하는 예방이 중요
고대성 수의사
Technical Manager
한국베링거인겔하임동물약품
수의학 박사
개 요
“면역억제(Immunosuppression)”는 면역체계에 일시적 혹은 영구적인 기능장애로 인해 선천성 면역 또는 획득(후천성) 면역반응이 정상적으로 작동하지 못하고 질병에 대한 감수성이 증가된 상태를 말한다. 최근 농장에 방역 수준이 상승되었을 뿐 아니라 백신접종 등 여러 예방책들이 적용되면서 많은 질병들이 일정 수준에서 관리되고 있는 반면 직접적으로 눈에 띄는 피해를 보이지는 않았던 면역억제현상이 재조명되고 있다.
닭이 면역이 억제된 상태에서는 여러 병원체의 감염에 취약해져 질병에 쉽게 걸릴 뿐 아니라 백신접종을 통해 기대할 수 있는 항체역가도 감소할 수 있다. 따라서 이번 글에서는 주요 면역억제 질병인 마렉병과 감보로병의 면역억제현상에 초점을 맞춰 알아보고자 한다.
닭의 면역장기와 면역체계
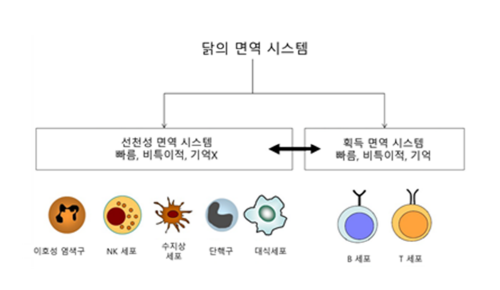
면역억제질병이 타깃으로 하는 닭의 면역계는 크게 천성/후천성 면역으로 구분할 수 있다(그림 1). 선천성 면역반응의 특징은 빠르고 비특이적(non-specific)이라는 점이다. 외부에서 침입한 병원체에 대해 즉각적으로 반응하여 병원체를 사멸하기 위해 여러 면역세포가 작동하며 이후에 보다 특이적인 후천성 면역체계가 작동할 수 있도록 병원체의 정보를 제공하는 역할도 한다. 후천성 면역체계는 이러한 정보를 받아 특정 병원체에 대해 작동하는 높은 수준의 면역반응을 말한다.
하나의 예로 백신접종으로 특정 항원에 대해 특이적인 면역반응을 유도하는 것은 후천성 면역체계를 자극하는 것이며, 각각 작동하는 면역세포가 어떤 것인지에 따라 세포성 면역(T cell 위주), 체액성 면역(B cell 위주) 등으로 구분되기도 한다. 또한 이러한 면역세포들이 생성되고 성숙하며 주로 활동하는 장소가 닭에서의 면역장기라고 할 수 있는데 F낭, 흉선, 비장이 전반적으로 이러한 기능을 담당한다. 그리고 외부환경과 접촉이 잦은 결막, 비강, 기관지, 장관계에 국소적으로 분포하여 면역반응을 담당하는 여러 면역장기들도 존재한다.
그림 1. 닭의 면역체계
마렉병(Marek’s disease)
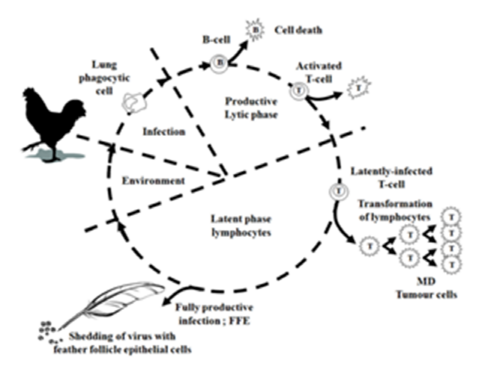
우리는 흔히 마렉병에 의한 피해로 마비증상과 내부장기의 종양형성 등으로 인한 도태 및 폐사를 생각하게 되는데, 마렉병 감염으로 인한 면역억제현상은 눈에 보이지 않고 확인이 어렵기 때문에 간과할 수 있다. 그림에 나와있는 경로와 같이 마렉병 바이러스는 호흡기를 통해 감염되며 먼저 폐의 대식세포에 의해 감작된 후 차례로 B 세포와 T 세포를 감염시켜 나가는데 이러한 과정에서 면역억제현상이 발생하게 된다(그림 2).
그림 2. 마렉병 바이러스 감염 과정
〈장형관 외, 2008〉
발생시기에 따라 초기면역억제(Early-MDV-IS), 후기면역억제(Late-MDV-IS)로 구분할 수 있는데 초기면역억제현상은 바이러스의 감염과정에서 B cell과 T cell이 감염되어 세포자멸사(apoptosis)가 발생하면서 나타난다. 이것은 위에서 말했던 면역기능을 하는 면역세포들이 파괴되는 것으로 당연히 면역력에 저하가 발생하게 된다. 연구에 의하면 마렉병 백신이 잘 접종된 상황에서는 초기면역억제에 의한 영향은 크지 않은 것으로 보인다.
하지만 운송 및 접종준비 중 여러 요인으로 인해 백신의 질(Quality)이 유지되지 않거나 접종의 미스가 발생하게 되면 면역억제에 의한 피해가 발생할 수 있다. 초기면역억제 현상은 육안으로는 면역장기의 위축으로 관찰되며 면역세포의 수 역시 감소하게 된다. 후기면역억제현상은 다시 잠복감염 후 재활성화과정(Late-MDV-IS-R)과 연관되었는지, 종양형성(Late-MDV-IS-T)과 관련되었는지에 따라 구분할 수 있다.
마렉병 바이러스는 T 세포 감염 후 잠복감염(latent infection)되는데 잠복감염되었던 바이러스가 다시 검출되는 것을 바이러스가 재활성화 되었다고 한다. 재활성화 중에 발생하는 면역억제현상은 면역장기의 위축과는 관련성이 낮은 것으로 알려져 있으며 ILT 백신의 효능을 떨어뜨린 사례가 보고된 바 있으나 아직 실체가 명확하게 밝혀지지는 않았다.
한편 후기 면역억제현상 중 종양형성 중 발생하는 면역억제현상은 만들어지는 종양에서 분비되는 다양한 세포인자들이 면역력세포와 면역체계가 작동하는 것을 방해하면서 나타나게 된다.
이미 2000년대 초반 마렉병 바이러스의 병원성이 증가하였다는 연구결과(mild MDV, virulent MDV, very virulent MDV, vv+MDV)가 있었으며(그림 3), 병원성이 강할수록 면역억제현상이 더욱 확연하게 나타난다는 여러 결과들이 뒤이어 발표되었다.
그림 3. 마렉병 바이러스의 병원성 증가와 그에 따른 백신주의 사용
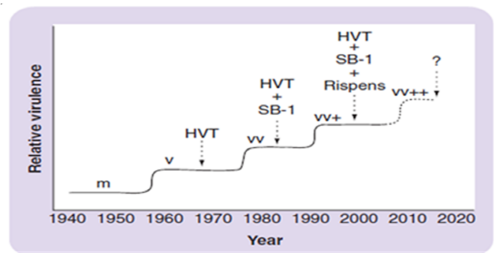
〈Adapted from R.L Witter, 1998〉
따라서 마렉병에 의한 가시적인 일차 피해뿐 아니라 면역력 저하로 인한 이차적인 피해도 늘어날 우려가 있어 이에 대비하는 것이 필요해 보인다. 올바른 백신접종은 마렉병 예방에 가장 현실적이고 효과적인 대응 방법이다. 관련 수의사와 협의 하에 품질(quality)이 유지된 백신이 정량으로 접종될 수 있도록 하는 것이 매우 중요하다.
전염성 F낭 병(Infectious Bursal Disease)
전염성 F낭 병 바이러스(Infectious Bursal Disease virus, IBD)의 감염으로 발생하는 이 질병은 국내 농가에도 널리 알려져 있다. 하지만 전염성 F낭 병에 의한 피해는 주로 관련된 임상증상 즉, 설사, 근육 출혈이라든지 F낭의 출혈 및 괴사 등 주로 육안병변으로 인식되고 있다. 실제 닭이 폐사하는 상황에서는 이러한 임상증상이 동반되는 경우가 많지만 전염성 F낭 병은 준 임상형 감염으로 면역억제현상을 일으키기도 한다.
그림 4. 전염성 F낭 병 감염에 의한 F낭의 조직병변 (좌) 정상적인 F낭의 모습, (우) 스코어 5(가장 심한 병변)
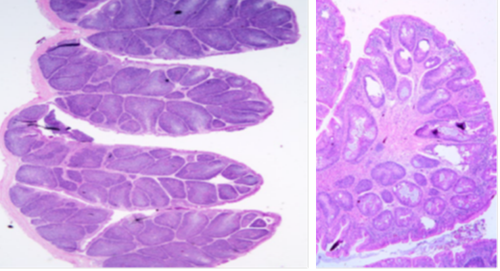
〈Frederic J. Hoerr, 2019〉
전염성 F낭 병 바이러스가 닭의 체내에서 증식하는 장소는 F낭 안에 있는 면역세포인 B림프구이다. 따라서 감염된 B림프구와 차례로 감염되는 주위의 세포들은 세포자멸사(apoptosis) 과정을 통해 죽게 되고 점차 F낭 안에 B세포의 수는 점차 감소하게 된다. IBDV 감염으로 인한 세포의 파괴는 조직사진을 보면 쉽게 구분할 수 있는데 병변이 심한 경우 구멍이 뚫린 것과 같이 내부가 비어 있는 것을 볼 수 있다(그림 4).
B세포는 외부 항원을 인식하여 다른 면역세포들에게 제시하거나 특정병원체에 대한 항체를 생성하는 기능을 하는데 B세포가 파괴됨으로 인해 정상적인 면역반응이 이뤄지지 않게 되고 면역저하가 발생하게 된다. 특히 항체를 생성하는 기능이 저하된다는 것은 감염되는 여러 병원체들에 대한 기본적인 방어능력의 저하 뿐 아니라 백신접종으로 인해 기대할 수 있는 항체역가도 낮아진다는 것을 의미한다.
항체형성능력이 저하되면서 단지 전염성 F낭 병에 대한 항체뿐 아니라 육계에서 주로 사용되는 ND, IB 등에 대한 항체형성능력 역시 저하될 수 있다. 산란계, 종계의 경우 보다 여러 종류의 백신들이 사용되며 면역저하가 장기간 피해를 줄 수 있기 때문에 이러한 피해는 더욱 커질 수 있다.
한편 최근에 국내 육계에서 많이 검출되는 것으로 알려진 전염성 F낭 병 바이러스인 G2d 변이주는 경우에 따라 임상증상은 심하게 나타나지 않지만 면역억제현상을 일으키는 준임상형 감염을 일으키는 것으로 알려져 있다(그림 5).
전염성 F낭 병 방어를 위해 생백신과 사백신이 활발히 사용되고 있다. 생백신은 편의상 중간독, 중간독 플러스로 구분하는데 중간독 플러스 백신은 모체이행항체를 극복할 수 있는 능력이 더 큰 반면 F낭에 미치는 영향은 중간독에 비해 더 크다.
그림 5. 국내 육계 농가에서의 전염성 F낭병 검사결과
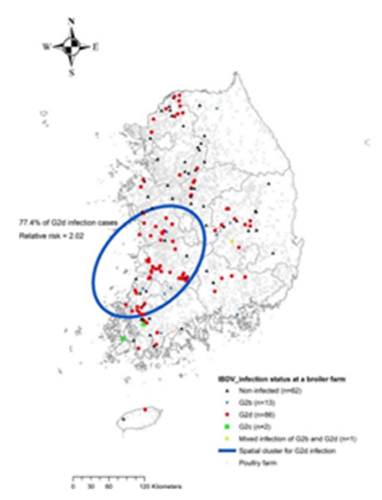
〈(Tuyet Ngan Thai 외, 2022, viruses), G2d 타입의 변이주가 가장 높은 빈도(n=86)로 검출되는 결과를 확인할 수 있다. 〉
따라서 중간독 플러스 백신은 감보로병 감염위협이 더 높은 상황에서 사용하고 중간독 백신은 보다 안정된 상황에서 사용하는 것이 일반적이다. 다만 이러한 구분은 단순화시키기 어렵기 때문에 사용백신의 선택은 반드시 수의사와의 지도 하에 이루어져야 한다.
면역억제 평가
그렇다면 닭이 면역억제 상태인지 아닌지 어떻게 평가할 수 있을까? 마렉병, 감보로병이 강력하게 의심된다면 면역억제현상이 있을 것으로 추정해 볼 수 있지만, 그런 상황에서는 눈에 띄는 피해가 발생하기 때문에 면역억제현상 여부에 대한 판단은 크게 중요하지 않을 수도 있다.
따라서 준임상형 감염 시 면역억제 여부에 대한 판단에 관심을 가지게 되는데 필드 상황에서 이러한 평가는 녹록지 않다. 혈중 헤테로필:림프구의 비율, 면역력과 관계된 사이토카인(Cycokine)인 인터페론 감마(IFN-γ)나 인터페론 알파(INF-α)가 얼마나 만들어지는 알 수 있는 mRNA 수준 평가 등 일반적으로 필드와 실험실에서 행해지는 검사 방법은 아니기 때문이다. 따라서 면역억제 질병은 무엇보다 백신접종을 골자로 하는 예방이 중요하다고 말할 수 있다.
벡터백신의 사용
위에서 말한 두 가지 질병을 한 번에 예방하기 위한 재조합 벡터백신이 적용될 수 있다. 이것은 예방을 목적으로 하는 병원체의 유전자 일부(A)를 다른 바이러스(B)에 삽입하여 제작된 백신으로, B가 체내에서 증식하면서 동시에 B에 포함된 A로부터 만들어진 단백질이 면역반응을 유도하는 방식이다.
현재 사용되고 있는 벡터백신은 마렉병 바이러스인 HVT에 전염성 F낭병 바이러스의 유전자인 VP2가 삽입되어 있는 HVT+IBD(VP2) 벡터백신이다. (HVT+IBD(VP2) 백신은 18 일령 종란에 인오보 접종하거나 1 일령 병아리에 피하접종하게 되며 HVT와 IBD에 대한 면역력을 함께 획득할 수 있다. 또한 허피스 바이러스인 HVT의 특성상 잠복감염(latent infection)하며 여러 요인에 따라 평생 동안 재활성화 되므로 한 번 백신을 했을 때 면역 지속기간이 매우 길다는 장점이 있다.
또한 전염성 F낭 병 생백신은 모체이행항체 수준을 고려하여 백신 바이러스가 영향을 덜 받도록 접종일을 정해야 하는데 벡터백신은 이러한 부분에서 자유롭게 된다. 한편 이러한 HVT+IBD 접종 후 전염성 F낭 병 ELISA로 항체 수준을 알기 위해서는 VP2 특이적인 항체를 검출할 수 있는 ELISA 키트를 사용해야 올바르게 항체역가를 평가할 수 있다. 또한 HVT+IBD 벡터백신을 사용 시 CVI988+HVT합제나 HVT 단독 등 HVT가 포함된 다른 백신과 함께 접종하는 경우 IBD 방어력이 저하될 수 있기 때문에 주의해야 한다.
두 바이러스의 복합감염
마렉병 바이러스와 전염성 F낭병 바이러스의 복합감염은 마렉병의 발생률을 증가시키는 것으로 알려져 있다. J. J. Giambrone 등의 연구에서 마렉백신을 하지 않은 계군에 전염성 F낭병 바이러스를 실험감염 시켰더니 마렉병의 발병률은 56.3%에 달한 반면 전염성 F낭병 바이러스를 감염시키지 않은 계군의 마렉병 발병률은 18.1%로 감소하였다.
또한 같은 실험에서 마렉백신 접종 후 전염성 F낭병 바이러스에 감염시킨 계군에서 마렉병 발병률은 20.7%로 나왔으며 마렉백신 접종 후 전염성 F낭병 바이러스에 노출되지 않은 계군은 2.99%의 낮은 발병률을 나타냈다. 이 결과는 마렉병 방어에 있어서 기본적으로 마렉백신의 역할이 중요하지만 전염성 F낭 병의 감염으로 인한 면역억제현상으로 마렉백신의 효능이 영향을 받을 수 있다는 점을 시사한다.
맺음말
앞서 말한 바와 같이 면역억제질병은 겉으로는 구분하기가 어렵고 실험실적 진단도 항체역가를 측정하는 것 외에는 제한적인 부분이 많다. 면역체계는 닭이 성장하는 과정 중 다른 신체기관들보다 우선하여 어린 일령부터 발달하기 때문에 면역억제 질병을 잘 컨트롤한다면 좋은 퍼포먼스를 보여줄 수 있는 기초가 완성되었다고 볼 수 있다. 부디 농가들이 면역억제증상으로 인한 피해를 받지 않기를 바라며 글을 마친다.